Un sistema termodinámico aislado alcanza el equilibrio cuando la entropía del sistema es máxima. Por ejemplo, el flujo de calor desde un cuerpo caliente a otro frío suponen un incremento de entropía. Este aumento tiene lugar hasta que los cuerpos alcanzan la misma temperatura (equilibrio térmico). El proceso de disolución de una sal en agua suponen un incremento de entropía, que cesa cuando toda la sal se ha disuelto.
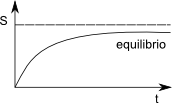
En un sistema aislado que no esté en equilibrio material, las reacciones químicas espontáneas, o el transporte de materia entre fases son procesos irreversibles que aumentan la entropía. Estos procesos continúan hasta que la entropía alcanza su valor máximo.
La condición de equilibrio material es la maximización de la entropía del sistema más la del entorno.
$\Delta S_{sis}+\Delta S_{ent}$ máxima en el equilibrio.
$\Delta S_{sis}$ es máxima en el equilibrio para sistemas aislados.



