La fórmula empírica indica los átomos que participan en el compuesto así como su proporción. Por ejemplo, la glucosa tiene de fórmula empírica CH2O, que nos indica la presencia de carbono, oxígeno e hidrógeno en su estructura en proporción 1:2:1. Sin embargo, la fórmula real de la molécula de glucosa es C6H12O6.
Fórmula molecular, es la fórmula real de la molécula, nos indica los tipos de átomos y el número de cada tipo que participan en la formación de la molécula. Por ejemplo, la fórmula molecular de la glucosa, C6H12O6, nos dice que cada molécula se compone de 6 átomo de C, 12 átomos de hidrógeno y 6 átomos de óxígeno.
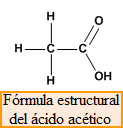 Fórmula estructural, muestra la forma en que se unen los diferentes átomos para dar lugar a la molécula. Por ejemplo, el ácido acético tiene de fórmula molecular, C2H4O2, que no indica como se unen los 8 átomos que componen la molécula. La fórmula estructural nos muestra que uno de los carbonos se une mediante enlaces simples a tres hidrógenos y al segundo carbono. Por su parte, el segundo carbono forma un enlace doble con el primer oxígeno y un enlace simple con el segundo que a su vez une a un hidrógeno.
Fórmula estructural, muestra la forma en que se unen los diferentes átomos para dar lugar a la molécula. Por ejemplo, el ácido acético tiene de fórmula molecular, C2H4O2, que no indica como se unen los 8 átomos que componen la molécula. La fórmula estructural nos muestra que uno de los carbonos se une mediante enlaces simples a tres hidrógenos y al segundo carbono. Por su parte, el segundo carbono forma un enlace doble con el primer oxígeno y un enlace simple con el segundo que a su vez une a un hidrógeno.
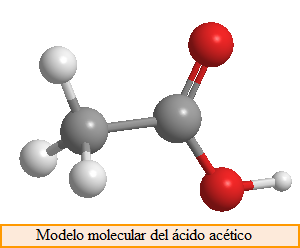 Por último, debemos considerar que las moléculas poseen una disposición espacial, son estructuras tridimensionales, y debemos utilizar modelos moleculares para respresentarlas de forma satisfactoria. Un modelo muy usado es el de bolas y barras que se muestra a continuación.
Por último, debemos considerar que las moléculas poseen una disposición espacial, son estructuras tridimensionales, y debemos utilizar modelos moleculares para respresentarlas de forma satisfactoria. Un modelo muy usado es el de bolas y barras que se muestra a continuación.



