La configuración electrónica de los átomos es clave para entender cómo se forman las moléculas. Gilbert Newton Lewis llegó a la conclusión de que los átomos se combinan para alcanzar la configuración electrónica de los gases nobles.
En la formación de un enlace entre das átomos sólo participan los electrones más externos, llamados electrones de valencia. Lewis diseñó un sistema para representar el átomo con sus electrones de valencia, que consiste en dibujar el símbolo del elemento rodeado de puntos, que representan cada uno de los electrones de valencia.
Ideas principales de la teoría de Lewis:
- Los electrones de valencia son los responsables de formar enlaces.
- Los electrones pueden transferirse entre átomos dando lugar a cationes y aniones que se atraen para formar compuestos iónicos.
- Cuando los electrones se comparten entre los átomos se forman enlaces covalentes
- Los electrones intercambiados permiten a los átomos adquirir la estructura electrónica de gas noble. Generalmente quedan rodeados de 8 electrones en su capa externa, llamado octeto.
Podemos saber fácilmente el número de electrones de valencia de un elemento fijándonos en el grupo de la tabla periódica al que pertenece.
Grupo 1 (alcalinos) tienen un electrón de valencia.
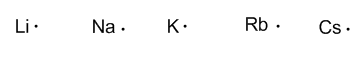
Grupo 2 (alcalinoterreos) tienen dos electrones de valencia.
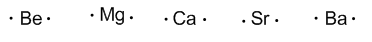
Grupo 13 (Boro, aluminio, galio, indio y talio) tiene tres electrones de valencia.
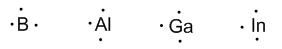
Grupo 14 (carbono, silicio, germanio, estaño y plomo) tiene cuatro electrones de valencia.
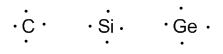
Grupo 15 (nitrógeno, fósforo, arsénico, antimonio y bismuto) tiene 5 electrones de valencia.
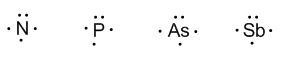
Grupo 16 (oxígeno, azufre, selenio y teluro) tiene 6 electrones de valencia.
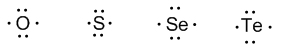
Grupo 17 (flúor, cloro, bromo y yodo) tiene siete electrones de valencia.
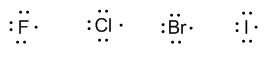
Grupo 18 (Neon, argon, kripton xenol y radon) tiene ocho electrones de valencia. La única excepción a esta regla es el Helio con dos electrones de valencia.



