Los metales alcalinos tienden a perder un electrón para alcanzar la configuración electrónica de gas noble, transformándose en iones positivos. Por otro lado los halógenos alcanzan dicha configuración al añadir un electrón a su capa de valencia, transformándose en iones negativos. La unión de iones positivos y negativos por fuerzas electrostáticas genera una red cristalina, un compuesto iónico.
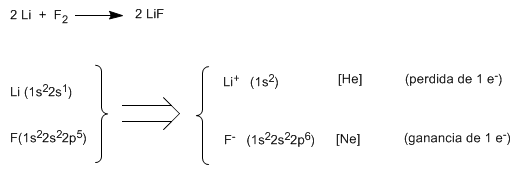
Así el fluoruro de litio (LiF) se obtiene cuando el litio (1s22s1) cede uno de los electrones de valencia al flúor (1s22s22p5), formándose el catión litio (1s2)y el anión fluoruro (1s22s22p6). Como puede observarse en las configuraciones electrónicas el catión litio es isoelectrónico al helio y el anión fluoruro isoelectrónico al neon.
Empleando símbolos de Lewis![]()
Veamos como segundo ejemplo la formación del óxido de calcio, CaO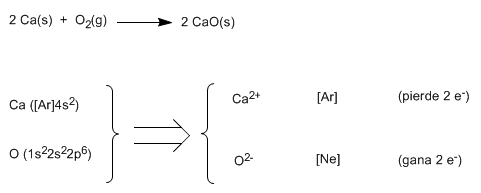
Empleando símbolos de Lewis:![]()



